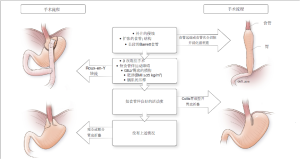
胃底折叠失败后的补救性旁路手术或胃窦切除Roux-en-Y吻合术
简介
胃食管反流病(GERD)在西方国家盛行,高达20%的成人病患每周都会出现相应症状[1]。虽然制酸疗法被普遍用于症状控制,但腹腔镜胃底折叠术仍是治疗胃食管反流病的金标准手段[2]。有报道称,大中心治疗该病长期的治疗效果非常好,5年、10年甚至20年,患者的满意度都超过90%[3,4]。然而,有些患者主诉症状反复出现,或出现令人不满意的新发症状,这些可能都需要再次手术干预[5]。而再次手术,最常见的术式是重做胃底折叠术,这与围手术期发病率和死亡率的增加有关,同时和不良的临床结局有关[6]。一些接受了二次手术的患者要么是不适合做基底折叠术,要么是由于不能耐受胃底折叠术而导致胃食管连接处(GEJ)或胃底的医源性创伤。这些患者都是行Roux-en-Y(RNY)重建或食管切除的较好人选[5,7-9]。
在现代腹腔镜发展的今天,RNY已经成为减肥手术的必要手段,但RNY重建术长期以来一直被用作抗反流术式,特别是运用于复杂的疾病治疗或胃底折叠手术失败后。胃空肠吻合的RNY重建术到近端胃囊袋(有或没有远端胃切除术)本身就是一个很好的抗反流的结构,因为它可以转移胆汁和反流物,同时去除反流物(即打破胃和食管的连续性)。人们可以争论RNY的相对应用价值,但对于胃食管反流疾病的患者来说,原位保留远端胃(如旁路手术)或切除远端胃(即远端胃切除术)的RNY重建手术之间,并无明显的生理性差异。
历史视角
在早期的胃肠道切除和重建手术探索中,外科医生努力保持着器官的“正常”顺序,即食道到胃到十二指肠。然而,为了控制疾病需要逐步演化出偏离正常解剖顺序的消化道重建方式。Billroth II手术是胃窦切除术后的重建技术,它涉及运用了环形胃空肠吻合术[10]。经典的en-Y重建是由Caesar Roux在1893年所描述的[11]。RNY手术在胃肠道手术中有部分应用,通过避免胆汁反流对Billroth II手术进行一些补充。
RNY胃空肠吻合术作为抗反流的方法,诞生时间早于抗胃酸分泌疗法。1956年,Ellis在手术诱导的反流疾病模型(即贲门切除术加食管胃吻合术)中运用了RNY胃空肠吻合术,并表明这是一种治疗复杂反流性食管炎可行的方案[12]。在1984年,Washer等人发表了一项随机研究的结果,试验比较了Nissen胃底折叠术和胃窦切除合并RNY吻合。Washer等人的研究表明,对于不可复原的食管裂孔疝和再次手术的病例,胃窦切除合并RNY吻合是更好的选择。Ellis后来将自己34年的临床经验总结并发表,他对需要再次手术的复杂胃食管反流患者进行了RNY手术,并展示了瞩目的治疗成功率[13]。Csendes等人发表了几份继续使用旁路手术作为抗反流手段的工作总结,包括针对正常患者和肥胖患者的治疗。2002年他报告了210例Barrett食管的患者接受部分迷走神经及胃切除合并十二指肠转流手术的长期随访资料,并报告了令人瞩目的临床结果[14]。Braghetto等人推进了他的工作,他对肥胖患者治疗反流的三种术式进行了前瞻性比较,报告了以下结果——校准的胃底折叠术与胃后方固定术;胃底折叠术与迷走神经切断术,远端胃切除术和RNY胃空肠吻合术,腹腔镜RNY胃旁路手术。Braghetto等人发现在两个旁路手术组中的临床结果和体重下降都有显著性差异[15]。
胃底折叠术加远端胃切除术或不加胃底折叠术的次全胃切除术,是临床上可被接受的复杂胃食管反流疾病的最终治疗方案。前者对严重胃排空延迟的患者更有用,后者对无法实施胃底折叠术的患者更有效(如胃底受损或动力障碍的患者,特别是短食管或者无蠕动的食管)。
RNY胃旁路术作为一种减重手术的广泛应用,揭示了它对改善胃食管反流病的一些作用[16]。在RNY胃旁路手术中,远端胃被保留在原位。这种保留远端胃并且为RNY胃空肠吻合术做好准备,是治疗反流初始手术和再次手术的可行选择。不进行远端胃切除的重建术使外科医生能够保留胃,以便在未来进行食管切除时作为重建管道使用,用于治疗因食管动力严重恶化或Barrett食管进展而进行的手术。这也避免了严重的十二指肠残端漏的发生风险,而这种情况通常可能发生在接受过胃部切除手术的患者身上。
胃底折叠再次手术相关的风险因素
一些大型研究和荟萃分析表明,与初始抗反流手术相比,再次行胃底折叠术的患者所被报导的结果明显更差[6,17]。围手术期发病率和死亡率也更高[18]。下文将详细介绍可能导致胃底折叠再次手术后临床预后结局恶化的相关因素。
肥胖
体重指数(BMI)较高的患者腹腔压力也高,这给膈肌裂孔的闭合和胃底折叠术的缝线带来张力。据报道,病态肥胖(即BMI>35 kg/m2)与初始和再次胃底折叠手术术后的不良预后有关;然而,由于RNY与胃旁路术也应用于体重减轻的治疗,而且容易得到医疗保险机构的报销,因此经常在病态肥胖患者中进行应用。有趣的是,有几篇论文显示,体重指数较高(>40 kg/m2)的患者与体重指数在参考范围内的患者的临床结果相当[19,20]。
Akimoto等人之前报告,胃底折叠术后的失败与BMI有关[21],并发现BMI为30~35 kg/m2的患者和BMI为35 kg/m2的患者的失败模式相似,这些模式与BMI<30 kg/m2的患者不同。BMI>30 kg/m2而不是BMI>35 kg/m2的病例结果表明有类似的生理力量在发挥作用。在一个单独的回顾性分析中,Olson等人将患者报告的结果用线性BMI量表绘制出来,而不是比较分类的组别。BMI>32 kg/m2的患者再次行胃底折叠手术后的结果明显较差。无论绝对值是多少,BMI的增加似乎与再次行胃底折叠术后较差的临床结果有关;因此,对于肥胖的患者,应考虑采用其他抗反流手术(如RNY重建)[22]。
既往多次接受胃底折叠手术
如上所述,再次的胃底折叠术与较高的发病率和死亡率有关,同时所报告的临床结果也较差。胃底折叠术再次手术其负面结局的产生可能包括更普遍的短食管、食管动力障碍、胃排空延迟,以及迷走神经损伤风险的增加,和胃底的损伤。这些不良状况发生的可能性随着每次重新手术而增加。当患者经历了3次或更多的胃底手术,他们可能会增加迷走神经损伤和不良结局的风险[23,24]。我们也发现了类似的结果[25]。考虑将RNY重建作为再手术的首选是谨慎的,特别是如果最初的手术是在一个专业的中心进行。
短食管
成功的胃底折叠术要求将胃底部分或完全包裹在食管远端,食管远端必须无张力地位于膈肌下方。这需要腹腔内保留2~3 cm食管。食管活动后无法达到这一长度被称为短食管。Collis胃成形术加胃底折叠术是治疗短食管患者的首选术式。也许在前肠外科中,没有其他话题比短食管更能引起人们的争论。事实上,部分专家否认短食管的存在。然而,大多数外科医生都认为,短食管不仅存在,而且还必须通过胃底折叠手术去治疗。
短食管在再次手术中更为常见,这意味着在上次手术时错过了诊断。食管短小会导致不适当的张力,最终导致胃底折叠的失败。然而,Collis胃成形术加胃底折叠术的效果并不理想,在食管动力障碍的患者中尤其如此[26]。我们认为在再次手术的病例中,如果发现食管短小,特别是术前存在吞咽困难或检测显示食管动力差,既往又接受过胃底折叠术并涉及Collis手术的患者,再次行胃底折叠术很可能会导致不良的临床结局,而改行RNY是较为合适的选择。
食管蠕动障碍
部分患者,尤其是硬皮病患者,会出现严重的食管运动障碍和顽固的胃食管反流。据报道,与部分胃底折叠术相比,RNY重建术是更优的选择。在控制硬皮病患者的反流方面,RNY也优于食管切除术[27]。在这些患者中,中度或重度运动障碍的发生率较高,特别是那些食管较短或以前接受过一次以上胃底折叠术的患者,这类病例应考虑进行RNY重建。此外,由于运动障碍可能随着时间的推移而恶化,最终需要进行食管切除术,因此必须将远端胃留在原位。
GEJ或胃底的破坏
再次手术需要在重新进行胃底折叠术或RNY转换术之前,将之前的胃底折叠术和食管远端完全游离。接受再次手术的患者往往有致密的粘连,手术的分离会导致GEJ、胃底或两者的全层或浆肌层的损伤。虽然较小的缺损(尤其是在胃底)可以通过简单修补来处理,但较大的缺损则将导致无法进行胃底折叠术。在这种情况下,最好是进行RNY重建,即使RNY需要食管空肠吻合。在早期手术中使用网状补片,包括可吸收的生物合成网状材料,都会增加切除时损伤GEJ和胃底的风险;事实上,在这种情况下很有必要转为RNY手术[28]。
胃排空延迟
在大多数胃排空延迟的患者中,因其他原因(如上面列出的原因之一)而行RNY转流手术的需考虑行胃切除。而胃排空延迟的患者,特别是既往行幽门成形术后持续存在排空延迟的患者,最好进行RNY转流手术。对于出现胃排空延迟但没有上述其他影响因素的患者,重新进行胃底折叠术和远端胃切除术是获得治疗良好效果的优选。
如何进行RNY转流手术
RNY转流的抗反流手术包括3个不同的步骤:(Ⅰ)拆除以前的胃底折叠;(Ⅱ)恢复腹段食管的长度并且保持膈肌裂孔的闭合;(Ⅲ)RNY重建,伴或者不伴远端胃切除术。完全拆除之前的胃底折叠术并复原食管后,关闭膈肌裂孔,并在术中进行食管胃十二指肠镜检查(EGD),以评估复原手术是否彻底并排除操作对GEJ或胃底的损伤。如果下一步是进行性RNY转流手术,则不需要做Collis胃成形术(对于短食管的病例)。另外补片加固并不是手术的关键,是否通过开腹手术或腹腔镜手术进行操作,是外科医生的偏好问题。对于有足够经验的外科医生,许多病例可以通过腹腔镜进行,这样做的好处是减少围手术期的疼痛和缩短住院时间。在极少数情况下,我们不得不进行左径胸手术把疝入胸腔内的胃重新回纳(在血管结构附近的深部穿透性溃疡所导致的胃穿孔已经愈合),然后再经腹部入路进行RNY转流手术。
RNY转流包括3个关键步骤:(Ⅰ)选择食管空肠或胃空肠吻合,包括近端胃的尺寸;(Ⅱ)确定RNY的胆道和消化道肠襻的长度;(Ⅲ)评估远端胃的处置,决定是否切除它或将其留在原位。具体实施的示意图见图1。
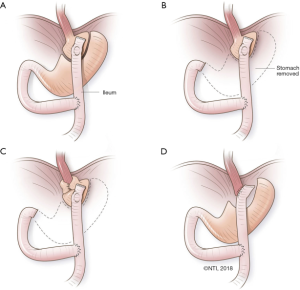
选择食管空肠或胃空肠吻合术,包括确定近端胃的尺寸
对于因手术复原或顽固性狭窄而对GEJ造成广泛损伤的患者,除了进行食管空肠吻合术外没有其他选择。我们建议使用沿胃小弯制备的近端胃,而不是横向穿过胃底。在传统的RNY减重手术中,近端胃囊非常小(即15~30 mL)。然而,在再次手术的病例中,制备一个更大的胃囊可能是更明智的选择。因为在切除过程中,最近端胃部在GEJ下面的血管可能会被破坏。此外,这种较小的囊袋可能与术后吞咽困难有关。
我们先评估小弯的血供,并在其下方至少4~5 cm处开始制备胃囊。如果复原先前的胃底折叠使得距离近端胃小弯附近几厘米血供流失,甚至可能是在角切迹处制备胃囊。在邻近胃小弯侧的小肠系膜上开一个洞。使用直线切割缝合器(45 mm)垂直激发吻合。直线缝合器的切割线平行于胃小弯,并超过His角。注意遵循胃小弯的弧度,以避免使最靠近的部分过于狭窄。胃囊囊袋的容量在60~100 mL之间,使患者能够吃到合理大小的食物。进行EGD检查是为了检查胃袋是否有破漏。
确定RNY的胆道输入肠襻和肠道输入肠襻的长度
对于传统的减重RNY胃旁路术,使用60 cm的胆道输入肠襻和100~150 cm的肠道输入肠襻。为了防止胆汁反流,有人提出消化道输入肠襻的最小长度为40 cm,在误差的情况下,即便是在胃恶性肿瘤的手术中,我们最常使用的肠襻长度为60 cm。胆道输入肠襻的长度并不影响胆汁反流。我们确定使用Treitz韧带向远端延伸的第一段肠段,这会比较容易提升至近端吻合的位置。这段肠子通常是15~20 cm长。用60 cm直线切割缝合器分割肠管。远端肠道被调整至到所需的消化道长度(至少60 cm),并在该水平与胆道输入肠襻的末端建立RNY吻合口。胆道输入肠襻以反收缩的方式被带到近端胃囊/食道旁边进行吻合。吻合后,再次进行EGD检查,以检查是否有破漏,并将胃管放置在吻合口上方。
评估远端胃的状况,选择是切除还是原位保留
我们尽可能原位保留远端胃,以减少手术时间和降低远端胃切除术并发症发病率,包括严重的十二指肠残端漏。在Barrett食管恶变或食管运动障碍进展的情况下,如果将来需要进行食管切除术,远端胃也可用于重建。此外,残胃可用于围手术期的胃造瘘,用于疾病复杂和全身情况差的患者药物和营养的输入。除了极端情况(如顽固性溃疡或远端胃的消化性狭窄),一般进行远端胃切除是不具备医学理由的。偶尔大弯侧的血管严重受损,远端胃不能作为未来的重建通道。在这种情况下,谨慎地进行胃切除术。图2总结了我们为患者量身制定的手术方案和决策全过程。
术后护理
RNY手术后,患者术后的管理方式与任何前肠手术后相同。我们通常在术后第1天(对于接受开放手术的患者会更晚)用水溶性造影剂进行放射性吞服造影。如果没有发现泄漏,就开始进行减重流质。我们通常会在患者排便后安排出院,患者此时已开始摄入流质饮食(说明如何避免高糖分食物)并接受了溃疡预防的相关治疗(即法莫替丁20 mg,每天两次)。
在接下来的2至3周内,患者将提前进入胃切除术后的饮食状态。我们建议患者每天服用多种维生素,并在术后6个月时进行营养学评估检查作为预防措施。尽管我们尚未发现新的营养缺陷(除了任何预先存在的缺陷)。一般在十二指肠或近端小肠吸收的药物(如左旋甲状腺素)的剂量需要随着时间的推移进行调整。从长远来看,患者和医生都必须关注内疝引起的闭合性肠梗阻。
RNY转流抗反流手术的结果
很少有研究专门报道RNY转流手术作为既往抗反流手术后的再手术治疗的临床结果。Ellis等人报告了一个由33名患者组成的研究组,这些研究人员采用了开放性方法,在平均534个月的随访时间中,发病率为27%,而且症状控制良好(72%的患者)[29]。Awais等人报告了他们对105名抗反流手术失败的患者进行RNY转流的结果,描述了大量既往的接受过Collis胃底折叠术的患者(即26%)。在这个研究中,46%的患者既往有2次或更多的手术史。Makris等人报告了一组72名接受过RNY转流手术的患者,并进行了长达5年的随访。他们报告了患者术后烧心、反胃和吞咽困难的症状均明显改善。在他们的研究中,一部分术前体重过轻的患者在症状缓解后体重增加,而病态肥胖的患者的体重则有所减轻[6]。Mittal等人报道过一个由130名接受再次胃底折叠术和RNY转流术的患者组成的大型研究组,发现两组患者的症状控制和患者满意度相当,尽管与再次胃底折叠术组相比,RNY组的不良结局的危险因素的发生率明显较高。但接受RNY的患者比第三次或更多次接受再次胃底折叠术的患者有更好的临床结果[8]。Juhasz等人报告说,在接受复发性食管裂孔疝超过5 cm的再手术的患者中,RNY转流术比重做胃底折叠术效果更好。他们认为这是因为在这一亚组的患者中,短食管的可能性较大[30]。Singhal等人报告了一个初次和再次手术的大型研究组,并描述了RNY转流术作为首选再次手术的比例明显更高。
结论
总的来说,再次进行抗反流手术或考虑RNY转流时,需要考虑多个因素。我们认为RNY对以前接受过抗反流手术的患者来说是改善症状的一种手段。对于一些有网状补片侵蚀、长段Barrett食管(和年轻病例)、食管扩张合并严重食管运动障碍并且无法进行扩张的狭窄患者,唯一的手术选择是远端或次全食管切除术,并进行消化道重建。
我们的手术计划和步骤大致遵循图2中的图示。总的来说,存在几种再手术干预的选择,并根据患者的症状、潜在的生理学和术中的发现所制定的不同方案。我们认为,对于需要再次手术的患者、短食管的患者(尤其是运动能力差)、严重食管运动障碍、胃排空延迟、BMI>32 kg/m2(对于BMI>35 kg/m2的患者更应如此)、体积大的复发型的食管裂孔疝的患者,RNY转流是一种更好的选择。当GEJ或胃底在术中受损时,RNY转流则是唯一的选择。
Acknowledgments
The authors wish to thank Clare Sonntag for her editorial assistance.
Funding: None.
Footnote
Provenance and Peer Review: This article was commissioned by the Guest Editor (Luigi Bonavina) for the series “Gastroesophageal Reflux Disease” published in Annals of Esophagus. The article has undergone external peer review.
Conflicts of Interest: Both authors have completed the ICMJE uniform disclosure form (available at http://dx.doi.org/10.21037/aoe.2018.08.02). The series “Gastroesophageal Reflux Disease” was commissioned by the editorial office without any funding or sponsorship. The authors have no other conflicts of interest to declare.
Ethical Statement: The authors are accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), which permits the non-commercial replication and distribution of the article with the strict proviso that no changes or edits are made and the original work is properly cited (including links to both the formal publication through the relevant DOI and the license). See: https://creativecommons.org/licenses/by-nc-nd/4.0/.
References
- El-Serag HB, Petersen NJ, Carter J, et al. Gastroesophageal reflux among different racial groups in the United States. Gastroenterology 2004;126:1692-9. [Crossref] [PubMed]
- Rickenbacher N, Kötter T, Kochen MM, et al. Fundoplication versus medical management of gastroesophageal reflux disease: systematic review and meta-analysis. Surg Endosc 2014;28:143-55. [Crossref] [PubMed]
- Draaisma WA, Rijnhart-de Jong HG, Broeders IA, et al. Five-year subjective and objective results of laparoscopic and conventional Nissen fundoplication: a randomized trial. Ann Surg 2006;244:34-41. [Crossref] [PubMed]
- Granderath FA, Kamolz T, Schweiger UM, et al. Long-term results of laparoscopic antireflux surgery. Surg Endosc 2002;16:753-7. [Crossref] [PubMed]
- Awais O, Luketich JD, Schuchert MJ, et al. Reoperative Antireflux Surgery for Failed Fundoplication: An Analysis of Outcomes in 275 Patients. Ann Thorac Surg 2011;92:1083-9; discussion 1089-90. [Crossref] [PubMed]
- Furnée EJB, Draaisma WA, Broeders IA, et al. Surgical reintervention after failed antireflux surgery: a systematic review of the literature. J Gastrointest Surg 2009;13:1539-49. [Crossref] [PubMed]
- Makris KI, Panwar A, Willer BL, et al. The role of short-limb Roux-en-Y reconstruction for failed antireflux surgery: a single-center 5-year experience. Surg Endosc 2012;26:1279-86. [Crossref] [PubMed]
- Mittal SK, Légner A, Tsuboi K, et al. Roux-en-Y reconstruction is superior to redo fundoplication in a subset of patients with failed antireflux surgery. Surg Endosc 2013;27:927-35. [Crossref] [PubMed]
- Awais O, Luketich JD, Reddy N, et al. Roux-en-Y Near Esophagojejunostomy for Failed Antireflux Operations: Outcomes in More Than 100 Patients. Ann Thorac Surg 2014;98:1905-11; discussion 1911-3.
- von Hacker VR. Zur casuistik und statistik der magenresectionen und gastroenterostomieen. Verhandlungen der Deutschen Gesellschaft fur Chirurgie 1885;14:62-71.
- Roux C. De la gastroenterostomie. In: Revue de chirurgie, 1893:402-3.
- Ellis FH. Experimental Aspects of the Surgical Treatment of Reflux Esophagitis and Esophageal Stricture. Ann Surg 1956;143:465-70. [Crossref] [PubMed]
- Washer GF, Gear MW, Dowling BL, et al. Randomized prospective trial of Roux-en-Y duodenal diversion versus fundoplication for severe reflux oesophagitis. Br J Surg 1984;71:181-4. [Crossref] [PubMed]
- Csendes A, Burdiles P, Braghetto I, et al. Early and late results of the acid suppression and duodenal diversion operation in patients with Barrett’s esophagus: analysis of 210 cases. World J Surg 2002;26:566-76. [Crossref] [PubMed]
- Braghetto I, Korn O, Csendes A, et al. Laparoscopic treatment of obese patients with gastroesophageal reflux disease and Barrett’s esophagus: a prospective study. Obes Surg 2012;22:764-72. [Crossref] [PubMed]
- Valezi AC, Herbella FAM, Schlottmann F, Patti MG. Gastroesophageal Reflux Disease in Obese Patients. J Laparoendosc Adv Surg Tech A 2018; [Epub ahead of print]. [Crossref] [PubMed]
- Little AG, Ferguson MK, Skinner DB. Reoperation for failed antireflux operations. J Thorac Cardiovasc Surg 1986;91:511-7. [PubMed]
- Singhal S, Kirkpatrick DR, Masuda T, et al. Primary and Redo Antireflux Surgery: Outcomes and Lessons Learned. J Gastrointest Surg 2018;22:177-86. [Crossref] [PubMed]
- Luketina RR, Koch OO, Köhler G, et al. Obesity does not affect the outcome of laparoscopic antireflux surgery. Surg Endosc 2015;29:1327-33. [Crossref] [PubMed]
- Martin Del Campo SE, Chaudhry UI, Kanji A, et al. Laparoscopic Nissen fundoplication controls reflux symptoms and improves disease-specific quality of life in patients with class I and II obesity. Surgery 2017;162:1048-54. [Crossref] [PubMed]
- Akimoto S, Nandipati KC, Kapoor H, et al. Association of Body Mass Index (BMI) with Patterns of Fundoplication Failure: Insights Gained. J Gastrointest Surg 2015;19:1943-8. [Crossref] [PubMed]
- Olson MT, Singhal S, Panchanathan R, et al. Primary paraesophageal hernia repair with Gore® Bio-A® tissue reinforcement: long-term outcomes and association of BMI and recurrence. Surg Endosc 2018; [Epub ahead of print]. [Crossref] [PubMed]
- Ellisjr F, Gibb S, Heatley G. Reoperation after failed antireflex surgery*Review of 101 cases. Eur J Cardiothorac Surg 1996;10:225-31; discussion 231-2. [Crossref] [PubMed]
- Papasavas PK, Yeaney WW, Landreneau RJ, et al. Reoperative laparoscopic fundoplication for the treatment of failed fundoplication. J Thorac Cardiovasc Surg 2004;128:509-16. [Crossref] [PubMed]
- Légner A, Tsuboi K, Bathla L, et al. Reoperative antireflux surgery for dysphagia. Surg Endosc 2011;25:1160-7. [Crossref] [PubMed]
- Bathla L, Legner A, Tsuboi K, et al. Efficacy and feasibility of laparoscopic redo fundoplication. World J Surg 2011;35:2445-53. [Crossref] [PubMed]
- Kent MS, Luketich JD, Irshad K, et al. Comparison of surgical approaches to recalcitrant gastroesophageal reflux disease in the patient with scleroderma. Ann Thorac Surg 2007;84:1710-5; discussion 1715-6.
- Stadlhuber RJ, Sherif AE, Mittal SK, et al. Mesh complications after prosthetic reinforcement of hiatal closure: a 28-case series. Surg Endosc 2009;23:1219-26. [Crossref] [PubMed]
- Ellis FH, Gibb SP. Vagotomy, antrectomy, and Roux-en-Y diversion for complex reoperative gastroesophageal reflux disease. Ann Surg 1994;220:536-42; discussion 542-3. [Crossref] [PubMed]
- Juhasz A, Sundaram A, Hoshino M, et al. Outcomes of surgical management of symptomatic large recurrent hiatus hernia. Surg Endosc 2012;26:1501-8. [Crossref] [PubMed]

孙志勇
上海交通大学医学院附属仁济医院胸外科。2005—2008年为上海第二医科大学附属仁济医院大外科住院医师,2008年至今在仁济医院胸外科工作。2018年在美国综合排名第一位的Mayo Clinic 研习胸外科微创手术及复杂食管外科手术及贲门失弛缓及GRED的外科治疗。2019年至上海肺科医院内镜中心研习支气管镜下的肺部肿瘤疾病诊断及腔道治疗。(更新时间:2021/8/9)
(本译文仅供学术交流,实际内容请以英文原文为准。)
Cite this article as: Kovacs B, Mittal SK. Remedial bypass or antrectomy and Roux-en-Y after failed fundoplication. Ann Esophagus 2018;1:8.